
文獻(xiàn)解讀

01研究介紹
熒光團(tuán)在非熒光狀態(tài)和熒光狀態(tài)之間的受控切換在每種超分辨率熒光顯微鏡技術(shù)中都起著關(guān)鍵作用落包,而探索全新的切換機(jī)制對于已有的和新興的超分辨率方法性能提升仍至關(guān)重要诸迟。在該研究中铲敛,作者提出了一種將3,6-二氨基氧雜蒽酮轉(zhuǎn)化為無籠基團(tuán)的光活化熒光團(tuán)的通用方法据德“旖埃可光活化的呫噸酮 (PaX) 在用光照射后能高效撵靴、清潔地轉(zhuǎn)化為高熒光蠕为、光和化學(xué)穩(wěn)定的吡咯啉染料诞昧。同時(shí)碉办,該策略也能擴(kuò)展到碳和硅橋聯(lián)的蒽酮類似物,產(chǎn)生一系列足以覆蓋大部分可見光譜的可光活化標(biāo)簽步嘹。研究結(jié)果證明了PaX染料在常規(guī)顯微鏡的固定細(xì)胞及活細(xì)胞標(biāo)記中具有多功能性和實(shí)用性虐干,以及在STED、PALM和MINFLUX的坐標(biāo)隨機(jī)和確定性納米觀察中的多功能性和實(shí)用性。
熒光納米顯微鏡以個(gè)位數(shù)納米分辨率實(shí)現(xiàn)了對具有分子特異性的生物樣品內(nèi)部結(jié)構(gòu)和動(dòng)力學(xué)的微創(chuàng)觀察际乘,大大提升了我們觀察(活)細(xì)胞的能力坡倔。而這些技術(shù)的核心在于化學(xué)特異性熒光標(biāo)記和熒光團(tuán)的開-關(guān)狀態(tài)之間的內(nèi)在控制。由于開關(guān)轉(zhuǎn)換不可逆的光活化染料或籠狀染料在使用時(shí)無需特定的成像緩沖液和高強(qiáng)度紫外線脖含,因此罪塔,它們在單分子定位顯微技術(shù)中被廣泛使用。如今光活化染料已被用于減少DNA涂料中的熒光背景养葵,并用于提高可通過通道疊加在受激發(fā)射損耗 (STED) 顯微鏡中同時(shí)成像的細(xì)胞結(jié)構(gòu)數(shù)量垢袱。其中,羅丹明染料因其光學(xué)和化學(xué)穩(wěn)定性港柜,細(xì)胞膜滲透性和亮度的顯著可調(diào)性请契,已成為熒光顯微鏡和納米顯微鏡中使用得最多的熒光團(tuán)之一,特別是硅羅丹明染料夏醉,因其出色的紅移發(fā)射爽锥、穩(wěn)定持久的熒光信號、良好的活細(xì)胞相容性和亮度而受到青睞畔柔。
在這之前匙杏,已報(bào)道的羅丹明的籠化策略一般都是依賴于以非熒光形式“鎖定”染料,即通過在氮原子上安裝耐光保護(hù)基團(tuán)(如硝基藜蘆基氧羰基或亞硝基)布橄,或者通過內(nèi)酯環(huán)合成轉(zhuǎn)化為相應(yīng)的環(huán)α-重氮酮充陷。然而,這兩種策略都存在一定的局限性荠涂,前者會(huì)降低染料的水溶性徊儿,并在光活化時(shí)產(chǎn)生潛在的毒副產(chǎn)物,而后者則會(huì)形成不同的非熒光副產(chǎn)物裙靶,導(dǎo)致主產(chǎn)物豐度降低泼剩。因此,在熒光顯微術(shù)和納米技術(shù)中犹喜,如果要求光活化能夠以快速的瓜释、完全的并且沒有副產(chǎn)物的方式進(jìn)行,那么無籠基的阎敬、緊湊型光活化的以及生物相容的熒光團(tuán)是非常必要的险锻。
02研究結(jié)果和討論
1、光活化標(biāo)簽的合成設(shè)計(jì)和機(jī)理
在這里魄帽,作者對反應(yīng)機(jī)理做出了猜想和驗(yàn)證(圖1b)现喳,PaX在受到405nm波長的光照后,由基態(tài)躍遷至激發(fā)態(tài)撕捍,與尚在基態(tài)的助劑上的孤對電子作用拿穴,使電子從助劑轉(zhuǎn)移到PaX上,之后通過烯烴上的電子轉(zhuǎn)移形成新的六元環(huán)忧风,經(jīng)過環(huán)內(nèi)電子轉(zhuǎn)移后默色,最后經(jīng)質(zhì)子化形成封閉式PaX-CF。
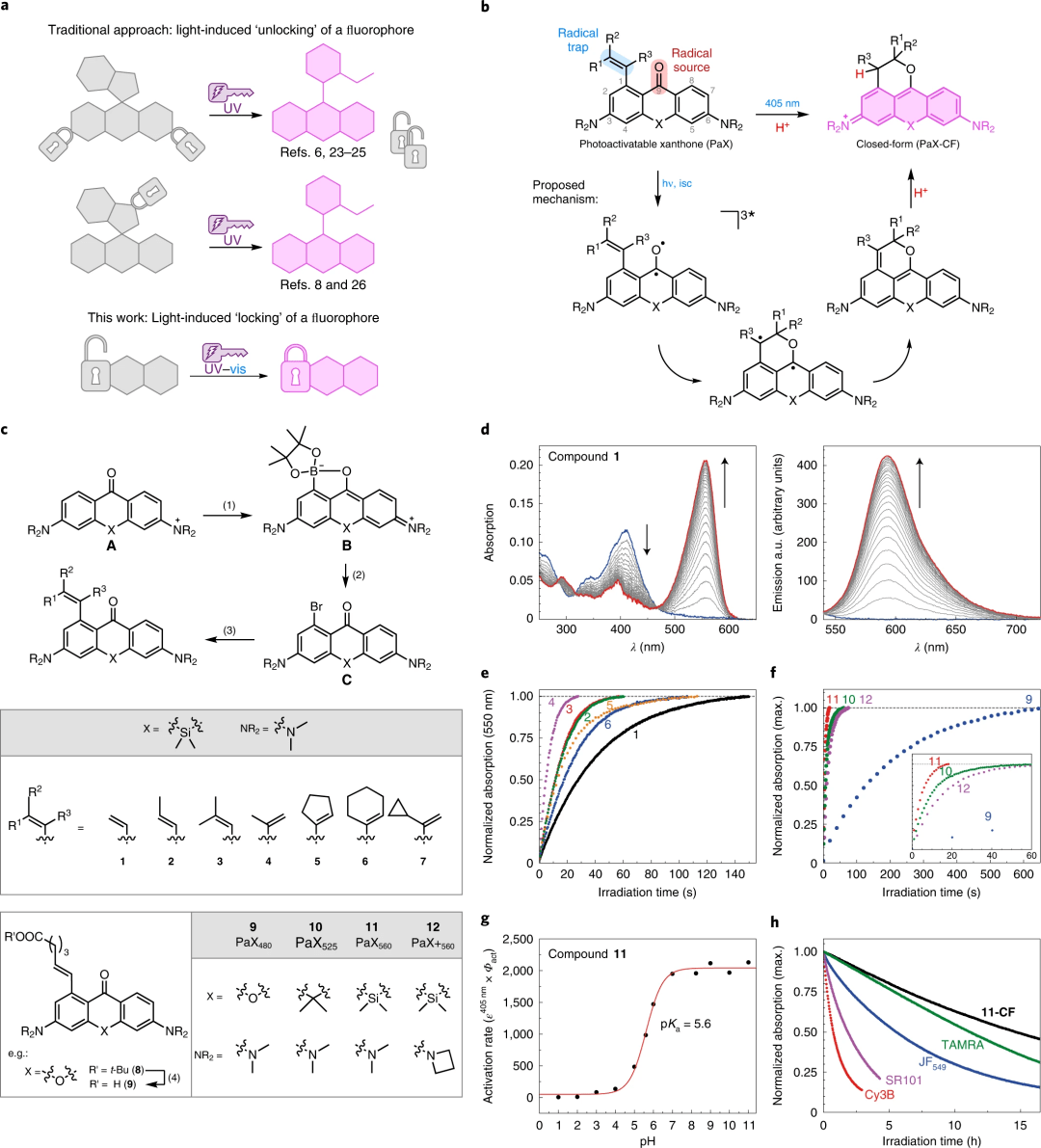
圖1狮腿、PaX染料的設(shè)計(jì)腿宰、合成和表征
a、作者采用了一種依賴于熒光團(tuán)的光誘導(dǎo)組裝 (“鎖定”)方法缘厢,在傳統(tǒng)方法中吃度,用于納米鏡的光活化染料一般依賴于籠狀基團(tuán)的釋放 (“解鎖”)。
b贴硫、具有1-烯基自由基阱及其9-烷氧基吡啶光產(chǎn)物 (閉合形式椿每,CF) 的PaX的一般結(jié)構(gòu),以及所提出的光激活機(jī)理英遭。
c砂腰、制備PaX的合成路線。
d蔑氛、在磷酸鹽緩沖液(100 mM潘娄,pH 7;λact = 405 nm)中化合物1 (1.66 μg ml-1) 隨時(shí)間變化的吸收光譜和熒光光譜汇割。
e持拐、在與d中相同的條件下,比較硅橋PaX 1–6的光活化動(dòng)力學(xué)恋得。
f啰哪、在與d相同的條件下,比較PaX染料9-12的光活化動(dòng)力學(xué)此妙。
g膜却、比較化合物11 (3.8 μM) 在不同pH值 (λact = 405 nm) 的磷酸鹽緩沖液 (100 mM) 中的比較光活化動(dòng)力學(xué)。
h殃通、在磷酸鹽緩沖液(λexc = 530 nm)中測量具有相似光譜特性的 11-CF 和已建立的商業(yè)熒光團(tuán)的抗光疲勞性攘默。
為了研究自由基受體取代的影響,作者合成了一系列可光活化的Si-xanthones (1-7; 圖1c)昔搂。目標(biāo)產(chǎn)物是通過銥催化玲销,螯合輔助,鄰位選擇的二芳基酮C-H硼化反應(yīng)(A)制備的摘符。在KF作用下贤斜,經(jīng)CuBr2-吡啶體系將生成的硼酸酯(B)轉(zhuǎn)化為相應(yīng)的芳基溴(C),最后在標(biāo)準(zhǔn) Suzuki-Miyaura 交叉偶聯(lián)反應(yīng)條件下進(jìn)行一系列烯烴取代逛裤。
2瘩绒、用于納米鏡的無籠狀基團(tuán)的光活化標(biāo)簽
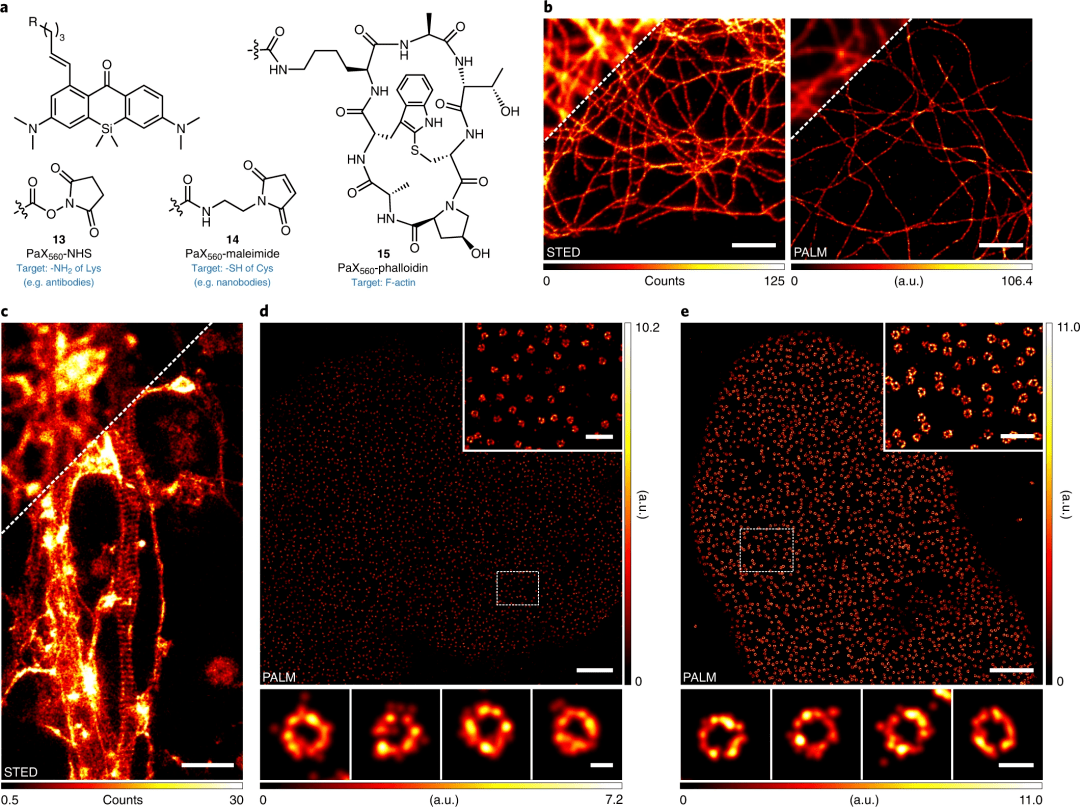
圖2猴抹、用于光學(xué)納米鏡的光激活標(biāo)簽
a、用于生物偶聯(lián) (13, 14) 和肌動(dòng)蛋白標(biāo)記 (15) 的PaX560衍生物的結(jié)構(gòu)锁荔。
b蟀给、COS-7細(xì)胞中微管的STED(左)和PALM(右)圖像,用帶有13的二抗間接免疫熒光標(biāo)記阳堕。
c跋理、固定的初級海馬神經(jīng)元培養(yǎng)物軸突中周期性膜細(xì)胞骨架的肌動(dòng)蛋白結(jié)構(gòu),用15標(biāo)記并置于Mowiol中恬总。
d前普、通過間接免疫熒光標(biāo)記的COS-7細(xì)胞中NPC的PALM圖像,用抗NUP98一抗和用 14標(biāo)記的二級納米抗體辱雅。
e麦荸、表達(dá)NUP107-mEGFP的HeLa-Kyoto細(xì)胞中NPC的PALM圖像,用與14偶聯(lián)的抗GFP 納米抗體標(biāo)記怨颜。
比例尺:2 μm(b-e经禽,主圖像),500 nm(d凫荡,e插圖)可剪,50 nm(d,底部)功抠,100 nm(e登翩,底部)。
3耘昙、用于活細(xì)胞成像的靶向標(biāo)簽
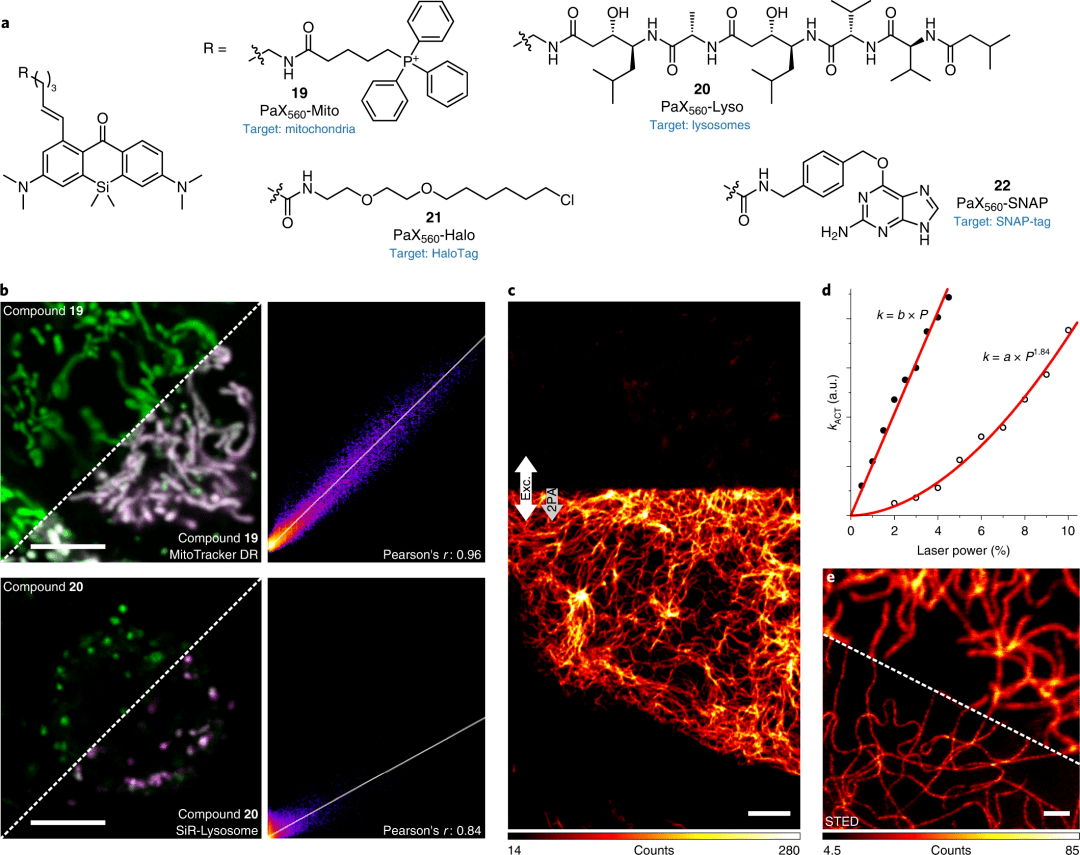
圖3沈路、在活細(xì)胞中使用可光激活PaX標(biāo)簽進(jìn)行成像
a、用于活細(xì)胞成像的PaX560衍生物 (19-22) 的結(jié)構(gòu)谓墨。
b加六、COS-7 細(xì)胞與19 (200 nM) 和 MitoTracker Deep Red (50 nM,上層) 或 20 (20 nM) 和 SiR-溶酶體 (200 nM怒见,下層)共孵育的共聚焦圖像和相應(yīng)的Pearson相關(guān)分析)俗慈。使用355 nm激光實(shí)現(xiàn)向19-CF和20-CF的轉(zhuǎn)換。
c遣耍、U2OS細(xì)胞中波形蛋白絲在激活前(上層)和雙光子激活(2PA)(下層闺阱,箭頭所示)標(biāo)記為21(200 nM)的共聚焦圖像。
d舵变、單光子(355 nm酣溃,100% 時(shí)為0.3 μW)或雙光子激活激光器(810 nm,10%時(shí)為109 mW)的激活率與激光功率的關(guān)系圖纪隙。
e赊豌、同一樣品在405 nm激光激活后的共焦(頂層)和 STED(底層)圖像扛或。
比例尺:5 μm (b,c)和1μm (e)。
4碘饼、通過選擇性光激活多路復(fù)用 PaX 標(biāo)簽
考慮到PaX染料的光活化速率的差異熙兔,作者推測兩個(gè)互補(bǔ)的標(biāo)簽可用于多路復(fù)用,依次應(yīng)用較低和較高劑量的激活光派昧,首先轉(zhuǎn)換一個(gè)熒光團(tuán)(例如PaX560),同時(shí)保留較難激活的熒光團(tuán)(例如PaX480 )颤皆,直到施加較高的光劑量酬苇。首先作者通過共焦成像測試了這一點(diǎn),然后通過雙色單檢測器 PALM成像在固定的細(xì)胞中測試给番,用細(xì)胞器(Pax560–Mito 19或Pax560–Lyso 20)和Halotag特異性(Pax480–Halo蚤件,23)標(biāo)記,通過共聚焦成像進(jìn)一步證明了活細(xì)胞中的順序激活狞绰。
03研究結(jié)論
作者引進(jìn)了一種無籠組完株、明亮和活細(xì)胞兼容的光活化染料的通用設(shè)計(jì)策略,適用于廣泛的光學(xué)顯微鏡和納米技術(shù)峦夺,包括PALM颁殃、STED和MINFLUX。這些PaX染料的獨(dú)特結(jié)構(gòu)特征將光響應(yīng)性3,6-二氨基呫噸酮核心與分子內(nèi)烯烴自由基阱功能化拄屈,從而提供高度緊湊且本身不帶電显钙、完整的細(xì)胞膜可滲透標(biāo)記。在單光子或雙光子活化下斋值,這些化合物迅速形成高度光穩(wěn)定的熒光吡咯啉染料绑雄。通過改變PaX染料的取代基,可以改變光活化動(dòng)力學(xué)以及光譜特性奥邮,從而實(shí)現(xiàn)多路復(fù)用偽彩色和傳統(tǒng)的多色成像万牺。
在固定和活細(xì)胞超分辨率熒光顯微鏡實(shí)驗(yàn)中,PaX染料的實(shí)用性和多功能性經(jīng)過各種目標(biāo)特異性探針和標(biāo)記策略得到了證明洽腺。這種方法將會(huì)進(jìn)一步刺激用于生物成像和材料科學(xué)的光活化探針和傳感器的發(fā)展脚粟。
(更多研究解讀將于后續(xù)分享)
04超高分辨率顯微成像系統(tǒng)iSTORM
寧波力顯智能科技有限公司(INVIEW)現(xiàn)已發(fā)布的超高分辨率顯微成像系統(tǒng) iSTORM,采用了源自諾貝爾化學(xué)獎(jiǎng)原理的 STORM 超高分辨率顯微成像技術(shù), 實(shí)現(xiàn)了光學(xué)顯微鏡對衍射極限的突破蘸朋,使得在 20 nm的分辨率尺度上從事生物大分子的單分子定位與計(jì)數(shù)珊楼、亞細(xì)胞及超分子結(jié)構(gòu)解析、生物大分子生物動(dòng)力學(xué)等的研究成為現(xiàn)實(shí)度液,從而給生命科學(xué)厕宗、醫(yī)學(xué)等領(lǐng)域帶來重大突破 。

圖4堕担、力顯智能自主研發(fā)的超高分辨率顯微成像系統(tǒng)iSTORM已慢。
超高分辨率顯微成像系統(tǒng) iSTORM 具有 20 nm超高分辨率曲聂、3通道同時(shí)成像、3D同步拍攝佑惠、實(shí)時(shí)重構(gòu)侠呛、2小時(shí)新手掌握等特點(diǎn),已實(shí)現(xiàn)活細(xì)胞單分子定位與計(jì)數(shù)凯践,并提供熒光染料選擇披锨、樣本制備、成像服務(wù)與實(shí)驗(yàn)方案整體解決方案符站, 以納米級觀測精度卖寻、高穩(wěn)定性、廣泛環(huán)境適用弯沥、快速成像除阐、簡易操作等優(yōu)異特性,獲得了超過50家科研小組和100多位科研人員的高度認(rèn)可鸳辛。
參考文獻(xiàn):
Lincoln, R., Bossi, M.L., Remmel, M. et al. A general design of caging-group-free photoactivatable fluorophores for live-cell nanoscopy. Nat. Chem. (2022).



